So sorgt Covid-19 für Chancen bei Medizinprodukten

Die Covid-19-Pandemie eröffnet Kunststoffverarbeitern neue Chancen, Medizinprodukte zu fertigen – doch die Branche ist reguliert.
Artikel für die persönliche Schutzausrüstung wie Schutzbrillen oder Medizinprodukte wie etwa OP-Masken: Mitte März hatte die EU einen Aufruf zu dringend benötigten Produkten zum Schutz gegen das Covid-19-Virus gestartet. Die Resonanz darauf von produzierenden Unternehmen, darunter auch Unternehmen der Kunststoffbranche, war riesig. „Bei uns alleine sind mehrere hundert Rückmeldungen eingegangen“, sagt Diethelm Carius, Referent der Arbeitsgemeinschaft Medizintechnik im VDMA. Man habe dabei allerdings auch einige Absagen erteilen müssen – zum Beispiel beim Angebot von Produktionskapazitäten oder von Produkte, die nicht in den Bereich der Schutzausrüstung fallen. „Auch kleine Unternehmen, die mithilfe additiver Fertigung ein paar Gesichtsmasken am Tag herstellen, haben wir an die örtlichen Gesundheitsämter verwiesen, da ihre Stückzahlen zu gering sind, um den Beschaffungsbedarf zu erfüllen“, so Carius.
Medizinprodukte benötigen CE-Kennzeichnung

Eine Herausforderung stellen für viele Kunststoffverarbeiter zudem Produkte dar, die als Medizinprodukte klassifiziert sind. „Diese benötigen eine CE-Kennzeichnung. Je nach Risikoklasse ist bei dem dafür notwendigen Konformitätsbewertungsverfahren die Mitwirkung einer Benannten Stelle notwendig“, erklärt Meinrad Kempf, Projektleiter beim Medizintechnik-Netzwerk Medical Mountains. Nur bei Medizinprodukten der Risikoklasse I dürfen Hersteller sich die Konformität selbst erklären. So können sie zum Beispiel das Zertifizierungsverfahren für OP-Masken eigenständig durchführen. Das heißt, sie beauftragen einen Sachverständigen, der den Prototypen anhand der Richtlinien für Medizinprodukte prüft und eine sogenannte Erklärung zur Konformitätsbewertung anfertigt. Diese müssen sie nicht beim Bundesinstitut für Arzneimittel und Medizinprodukte (Bfarm) einreichen, sondern nur bei eventuellen Kontrollen vorlegen.
Ab Risikoklasse IIa geht es nicht ohne Benannte Stelle
Ab der Risikoklasse IIa benötigen Hersteller aber für die CE-Kennzeichnung die Mitwirkung einer Benannten Stelle. „Der Weg dahin ist ein komplizierter Prozess, der auch die Produktionsprozesse umfasst und bei dem viele Normen und Standards einzuhalten sind“, so Kempf. „Von der ersten Idee bis zum Inverkehrbringen eines neuen Medizinprodukts dauert es zwischen zwei bis fünf Jahre. Das heißt, man braucht einen langen Atem“, stellt Carius klar. „Dass ein Unternehmen nun erstmals komplexe Medizinprodukte zu fertigen beginnt, die in der jetzigen Krise einsetzbar sind, ist aufgrund der strengen Regularien praktisch nicht vorstellbar.“ Kempf bestätigt dies: „Ein schneller Switch vom Automobil- zum Medizintechnikhersteller ist nicht möglich.“
Seat baut Beatmungsgeräte mit Sonderzulassung
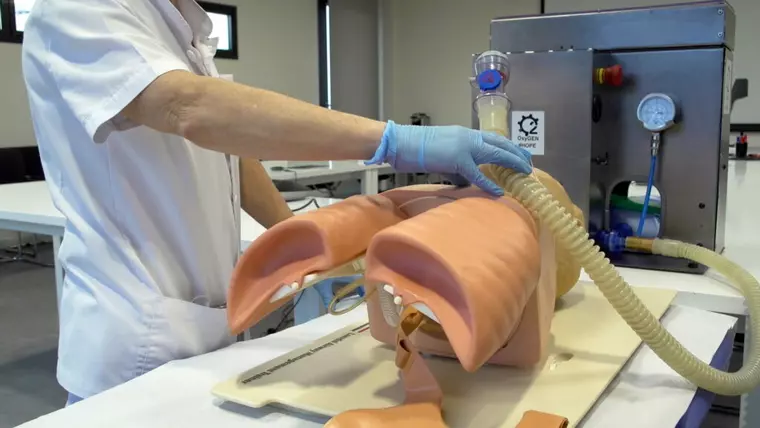
Doch Ausnahmen gibt es auch hier, wenn auch in Spanien: So montiert der zum Volkswagen gehörende Automobilhersteller Seat in einem Werk im spanischen Martorell nun Beatmungsgeräte statt Fahrgestelle für Autos. Die Beatmungsgeräte wurden gemeinsam mit einem Prototypen-Unternehmen aus Barcelona und der Unterstützung vieler Partner entwickelt – und inzwischen von der spanischen Zulassungsbehörde für Arzneimittel und Gesundheitsprodukte (AEMPS) für den klinischen Einsatz freigegeben.
Nikolas Kuczaty, Geschäftsführer der AG Medizintechnik im VDMA, geht davon aus, dass Beatmungsgeräten in Spanien dringend benötigt werden, sodass die spanischen Behörden hier eine schnelle Sonderzulassung ermöglicht haben.
Nach Zuliefererwechsel ist eventuell Neuzertifizierung notwendig
Auch die bloße Zulieferung von Bauteilen, die einer hohen Risikoklasse zugeordnet sind – wie zum Beispiel Schläuchen, die in die Lunge eingeführt werden – ist nicht problemlos möglich. Carius: „Ein Hersteller eines Medizinprodukts der Risikoklasse 3 wechselt nur ungern seine Zulieferer, weil er dann unter Umständen selbst eine neue Zertifizierung benötigt.“ „Kunststoffverarbeiter, die bei Medizinprodukten unerfahren sind, sollten sich nur mit unkritischen Komponenten und Bauteilen befassen“, rät Professor Christian Hopmann, Leiter des Institut für Kunststoffverarbeitung (IKV) an der RWTH Aachen.
Kein Wunder, dass Kunststoffverarbeiter, die bereits vor der Pandemie in der Medizintechnik tätig waren, nun ihre Produktionskapazitäten hochfahren. Dazu gehört beispielsweise BIW in Ennepetal, die Silikonschläuche für Beatmungsgeräte nun im Drei-Schicht-Betrieb fertigt und von der Bundesregierung als systemrelevanter Lieferant eingestuft wurde.
Neues Sonderzulassungsverfahren für Covid-19-Schutzmasken
Erleichterungen gibt es derzeit allerdings für Medizinprodukte im Bereich Infektionsschutzausrüstung, genauer gesagt Schutzmasken. Für sie hat das Bfarm am 6. April aufgrund des akuten Versorgungsengpasses ein Sonderzulassungsverfahren gemäß § 11 Abs. 1 des Medizinproduktegesetzes erlassen.
Cecimo fordert Sonderzulassung für additiv gefertigte Medizinprodukte

Sonderzulassungsverfahren fordert Cecimo, der europäische Verband der Werkzeugmaschinenindustrie, auch für Medizinprodukte, die additiv gefertigt werden. Entsprechende Hersteller, die ihre Hilfe bei der Herstellung von Schutzausrüstung angeboten haben, beklagen demnach, dass verschiedene regulatorische Anforderungen sie blockieren. Deshalb fordert Cecimo die politischen Entscheidungsträger auf, Additive-Manufacturing-Hersteller vorübergehend von den Anforderungen der Richtlinie über Medizinprodukte und Produkthaftung zu befreien.
„Die Hersteller wollen helfen, aber eine solche Sonderregelung halte ich für gewagt“, betont Carius. „Die Gesetzgebung schreibt aus gutem Grund eine sorgsame Validierung von Medizinprodukten vor“, sagt Hopmann. „Es dringend davon abzuraten, Produkte in Verkehr zu bringen, deren Wirksamkeit nicht gesichert ist.“ Kempf kann nachvollziehen, dass bei einem akuten Bedarf kurzfristig die Zügel gelockert werden. „Langfristig aber müssen die bestehenden Standards und Normen eingehalten werden.“
Corona-Drehscheibe bringt Anbieter und Nachfrager zusammen
Um die aktuellen Bedarfe und Angebote besser abgleichen zu können, hat Medical Mountains vor zwei Wochen auf seiner Webseite die sogenannte Corona-Drehscheibe gestartet, bei der alle Player im Bereich Medizintechnik – und solche, die es werden wollen – ihre Offerten und Nachfragen einstellen können. „Die Resonanz ist groß, das hat eine hohe Eigendynamik entwickelt. Und wir hoffen, dass dieser neue Spirit des Netzwerkens, der neue Ideen und Partnerschaften hervorbringt, auch nach der Pandemie erhalten bleibt“, stellt Kempf fest.
Auch der VDMA richtet seinen Fokus auf Innovationen durch übergreifende Zusammenarbeit: Er will laut Carius einen Arbeitskreis für das Thema Schutzausrüstung gründen, bei dem auch der Fachverband Kunststoff- und Gummimaschinen mit seinen Mitgliedsunternehmen mitwirken wird. Carius: „Letztlich geht es uns auch darum, den Standort Deutschland und Europa zu stärken.“
Sabine Koll
Passend zu diesem Artikel

Kunststofftechnik-Spezialist Oechsler investiert im Rahmen einer Wachstumsoffensive mehrere Millionen in den globalen Ausbau seiner Reinraum-Flächen.


